開立醫療多線產品獲得首張 MDR CE 證書
1970-01-01 08:33:43
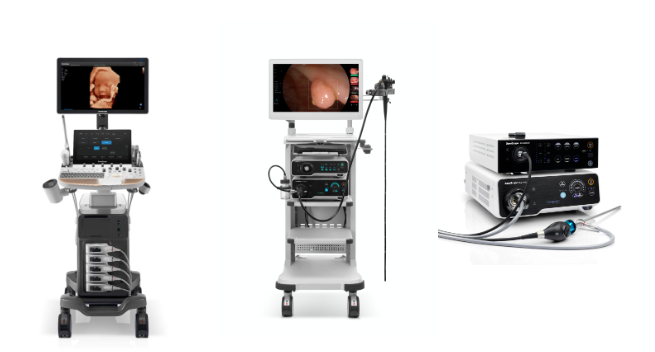
此次獲證的是開立自主研發的超聲、消化內鏡與腹腔鏡產品
CE認證是產品進入歐洲市場的“簽證”,獲簽的產品即符合與該產品相關的歐盟法律法規及標準。而MDR(EU 2017/745)是歐盟于2017年5月發布的新醫療器械法規,以替代原醫療器械指令MDD(93/42/EEC)。自2021年5月26日,MDR法規全面生效。
歐盟MDR新規更加關注臨床性能、更好的醫療器械可追溯性和對患者更大的透明度,給醫療器械制造商提出了更大的挑戰。相較于原MDD指令,MDR在產品的風險管理、產品的性能安全標準、上市前的臨床評價以及產品上市后的警戒和監管等方面提出了更高的要求。首張MDR證書的簽發再次印證了產品質量和技術團隊的高標準與高要求,體現了認證機構對開立醫療產品質量安全性和有效性、產品質量管理體系的極大認可。
歐洲市場作為超聲和內窺鏡產品準入門檻最高的市場之一,也是開立醫療海外拓展中的戰略重點。憑借品質過硬和技術融合創新的產品、歐洲市場的本地化營銷支持和銷售網絡、面向當地的本地化服務布局,開立醫療目前在歐洲市場取得了快速的業務增長和專家用戶的一致認可。

目前開立醫療已與歐洲多國的專家和醫院建立學術合作與交流,為歐洲用戶了解開立醫療的產品提供了窗口。同時,開立醫療在歐洲建立的自營服務中心提升了海外服務能力,保障了客戶滿意度以及對未來業務拓展的支持。

對于已經深耕歐洲市場多年的開立醫療來說,此次獲批首張MDR CE證書具有里程碑式的意義,為開立醫療進一步開拓歐洲市場、推動國際化進程打下了堅實的基礎。
